Формы специфического иммунного ответа
Содержание:
- Борьба с бактериями нейтрофилов
- Особенности гуморального иммунитета
- Физиология человека: Иммунная система
- Реакции гуморального иммунитета
- Прививка
- Система комплемента
- Разница между гуморальным и клеточным иммунитетом
- Неспецифический иммунитет
- Сила иммунного ответа
- Взаимосвязь клеточной и гуморальной защиты
- Клетки функциональной системы иммунного гомеостаза.
- Подробнее о Т-лимфоцитах
- Фазы нормального иммунного ответа во времени
Борьба с бактериями нейтрофилов
 Наиболее многочисленной армией белых клеток крови – лейкоцитов – являются нейтрофилы. Для целостной иммунной системы их работа крайне необходима, поскольку она направлена на уничтожение опасных болезнетворных бактерий в кровеносной системе, тканях.
Наиболее многочисленной армией белых клеток крови – лейкоцитов – являются нейтрофилы. Для целостной иммунной системы их работа крайне необходима, поскольку она направлена на уничтожение опасных болезнетворных бактерий в кровеносной системе, тканях.
Чтобы обозначить механизмы нейтрофилов в иммунной системе, выделим их два важнейших аспекта:
- Во-первых, нейтрофилы являются клетками-камикадзе системы самозащиты. Повстречавшись с бактерией, нейтрофил всасывает ее (фагоцитоз), разлагает в себе (лизис). Далее клетка погибает, выполнив защитную миссию.
- Во-вторых, нейтрофилы, как и другие группы белых клеток крови, имеют определенную норму в организме. Возрастание их количества (нейтрофилёз) легко выявляет общий анализ крови. К примеру, причинами нейтрофилёза (нейтрофилии) могут быть: абсцессы, туберкулез, сальпингит, алкогольная интоксикация и пр.
Обратите внимание, что незначительное повышение нейтрофилов не всегда является опасным сигналом для иммунной системы. Может наблюдаться при чрезмерной физической (умственной) нагрузке или после достаточно плотного обеда
Тщательная характеристика обстоятельств, повлекших их возникновение, позволяет правильно диагностировать возникшую патологию.
Особенности гуморального иммунитета
Данный иммунный механизм характеризуется выработкой антител к чужеродным микробам, химическим компонентам. В-лимфоциты имеют основную роль в . С их помощью происходит распознавание чужеродных агентов в организме. Затем начинается активная выработка антител (иммуноглобулинов) к чужеродным структурам.
Иммунные ответы на антигены могут быть классифицированы как первичные или вторичные ответы. Первичный иммунный ответ организма на антиген происходит в первый раз, когда он встречается. В зависимости от природы антигена и места входа этот ответ может занять до 14 дней для решения и приводит к генерации клеток памяти с высокой специфичностью для индуцирующего антигена. Гуморальный ответ, опосредуемый В-клетками с помощью Т-клеток, продуцирует высокоаффинные и антигенспецифические антитела.
Это имеет некоторые количественные и качественные отличия от основного ответа. Когда это нарушается, адаптивная иммунная система обеспечивает более эффективный ответ на очищающие патогены. Адаптивная иммунная система обладает способностью «запоминать» предыдущие антигены, процесс, называемый иммунологической памятью. Антигенспецифические Т-клетки выбираются во время первичного иммунного ответа и расширяются для получения клонов Т-клеток с высокой специфичностью для активирующего антигена. В первичной реакции В-клеток на тимус-зависимый антиген иммунная система выбирает В-клетки с высокой аффинностью и специфичностью для антигена, и они становятся ячейками памяти. Выбор В-клеток с высоким сродством к данному антигену происходит в зародышевых центрах вторичных лимфоидных фолликулов и требует индуцированной ферментами цитидиндезаминазы и взаимодействия с другими иммунными клетками. Во вторичной реакции на тот же антиген клетки памяти быстро активируются. Этот процесс быстрее и эффективнее первичного ответа. Врожденная иммунная система — первая линия защиты от инфекционных агентов.
. Ключевые слова: антигены; ячейки памяти; клональное расширение; зародышевые центры; созревание аффинности; переключение класса.
Выработанные антитела являются специфичными, они могут активно взаимодействовать только с чужеродными организмами, на которые среагировали.
Антитела могут находиться в крови, на клеточной поверхности, в грудном молоке, желудочной секреции и даже в слезах. За счет общего количества антител происходит формирование иммунной системы. Такое происходит после того, как человек перенес конкретное инфекционное заболевание или был привит. С помощью антител происходит нейтрализация токсических веществ, которые оказались в организме. К примеру, если проникает в организм конкретный вирус, антитела начинают блокировать рецепторы, поэтому он не поглощается организмом. За счет конкретных антител человек переносит легче конкретное заболевание или вовсе им не болеет.
Антиген-зависимые и независимые механизмы, которые поддерживают уровни антител к сыворотке. Филадельфия: Липпинкотт-Ворон. Отправьте примечание редактору об этой статье, заполнив форму ниже. Адаптивный иммунный ответ развивается медленнее, чем врожденный иммунный ответ, но он может действовать гораздо мощнее и быстрее, чем врожденный иммунный ответ против патогенов, которые он видел раньше. Адаптивный или приобретенный иммунный ответ на начальную инфекцию занимает несколько дней или даже недель, чтобы стать установленным, намного дольше, чем врожденный ответ.
Физиология человека: Иммунная система
- Иммунная система. Иммунная система человека. Неспецифический иммунитет. Специфический иммунный ответ. Рециркуляция лимфоцитов.
- Как укрепить иммунитет ребенка летом, чтобы он не болел зимой? Советы педиатра
- Что такое детский диатез и как помочь малышу?
- У человека склонность к аллергиям — как помочь пережить весну аллергику?
- На какие цветы чаще всего аллергия? Каких букетов следует опасаться
- Как предохранится от простуды и гриппа при беременности? Укрепляем иммунитет
- Как укрепить защитные силы организма? Повышаем иммунитет
- Всегда ли насморк и слезотечение это симптомы аллергии?
- Натуральные народные средства для укрепления иммунитета. Травы для здоровья
- Чем полезен лимон и зеленый чай с ним? Повышаем иммунитет
- Аллергия на пыльцу березы у ребенка. Кто в группе риска заболеть поллинозом?
Реакции гуморального иммунитета
Итак, что же получается, когда в наш организм проникает нечто “неправильное”, а клетки всеми силами стараются воспрепятствовать этому вторжению?
А получается реакция. И здесь мы рассмотрим основные виды реакций гуморального иммунитета.
Вообще правильнее будет называть это – иммунным ответом.
Первичный иммунный ответ
Возникает в тот момент, когда В-лимфоцит первый раз “встретился” с антигеном; он его “не знал” до этого момента. Поэтому ему нужно время на то, чтобы распознать, кто перед ним. Время это может составлять от 2 до 5 дней.
Примерно через 60 часов начинает синтезироваться IgM, а максимум выработки IgG достигается на 10 – 14 день. Также происходит увеличение уровней других иммуноглобулинов – A, E и D.

Для информации: процесс выздоровления начинается только тогда, когда уровень иммуноглобулинов дойдет до такого, который позволит нейтрализовать все токсины, выделенные патогенами. Отсюда вывод: чем раньше приступить к лечению болезни, тем меньше токсинов успеет выделить инфекционный агент и тем быстрее наступит выздоровление.
Вторичный иммунный ответ
Если В-лимфоцит “прогнал” патогена, а тот снова “явился” в организм, можно говорить о вторичном иммунном ответе, время которого будет значительно короче, чем первого. Дело в том, что в иммунологическую память записана некая информация во время изучения антигена, и если тот же самый антиген будет обнаружен во второй раз, информация будет извлечена из этой “памяти”.
Поэтому здесь разовьется следующая ситуация:
- даже если в организме мало антигенов, к ним всё равно будут образовываться антитела;
- выработка антител в исключительных случаях может произойти в течение одного дня;
- высокоспецифичные антитела IgG будут доминировать, за счет чего человек быстрее поправится.
Всем этим объясняется, почему дети сначала тяжело болеют, а потом, когда они на 3-4 раз столкнутся с тем же самым ОРЗ, болезнь будет протекать быстрее и, возможно, мягче. Это происходит не только потому, что иммунитет окреп, а еще и потому, что организму нужно предельно мало времени на распознавание “вредителя” и запуск программы по его ликвидации.
Прививка
Людям можно вводить мертвые или инактивированные формы опасного вируса или бактерии, которые будут стимулировать гуморальный иммунитет, не создавая никакой угрозы для организма.Если в какой-то момент в будущем этот человек подвергнется действию агента, должен последовать немедленный иммунный ответ, устраняющий его, прежде чем он сможет нанести серьезный ущерб.
Вакцинация более эффективна для некоторых видов инфекции. К сожалению, некоторые вирусы мутируют быстро, вызывая изменения соединений на их поверхностях, которые гуморальная иммунная система использует для их распознавания. Вот почему необходимо постоянно разрабатывать новые вакцины.
Люди, вакцинированные от стремительно мутирующего вируса, могут быть невосприимчивы к новому штамму, который появляется в следующем году, потому что химические вещества на его поверхности изменились и не будут признаны антигенами B-клеток организма.
Система комплемента
Система комплемента – комплекс белков, постоянно присутствующих в крови. Это каскадная система протеолитических ферментов, способных лизировать клетки, предназначенная для гуморальной защиты организма от действия чужеродных агентов, участвует в реализации иммунного ответа организма. Является важным компонентом как врожденного, так и приобретенного иммунитета.
Она активизируется реакцией антиген-антитело и необходима для опосредованного антителами иммунного гемолиза и бактериолиза, играет важную роль при фагоцитозе, опсонизации, хемотаксисе и иммунном гемолизе и необходима для усиления эффекта взаимодействия между специфическими антителами и антигеном.
Одной из причин снижения факторов комплемента в сыворотке крови могут являться аутоантитела, направленные против факторов комплемента. Снижение С3 и С4 компонентов комплемента сопровождается клинической картиной рецидивирующего кожного геморрагического васкулита и артралгией.
Уровень компонентов комплемента в крови варьирует в широких пределах. Наследственный дефицит компонентов комплемента или их ингибиторов может приводить к аутоиммунным нарушениям, повторным бактериальным инфекциям, хроническим воспалительным состояниям.
С3-компонент комплемента – центральный компонент системы, белок острой фазы воспаления. Это важнейшая часть защитной системы против инфекций. Он образуется в печени, макрофагах, фибробластах, лимфоидной ткани и коже. Вследствие активации С3 выделяется гистамин из тучных клеток и тромбоцитов, хемотаксис лейкоцитов и соединение антител с антигеном, поддерживается фагоцитоз, усиливается проницаемость стенок сосудов и сокращение гладкой мускулатуры. Активация С3 играет важную роль в развитии аутоиммунных заболеваний.
С4-компонент комплемента – гликопротеин, синтезируется в легких и в костной ткани. С4 поддерживает фагоцитоз, увеличивает проницаемость стенки сосудов, участвует в нейтрализации вирусов. Он участвует только в классическом пути активации системы комплемента. Увеличение или уменьшение содержания комплемента в организме наблюдается при многих заболеваниях.
Показания к исследованию
- Подозрение на врожденный дефицит комплемента, аутоиммунные заболевания, острые и хронические бактериальные и вирусные инфекции, (особенно рецидивирующие), онкологические заболевания;
- динамическое наблюдение больных с системными аутоиммунными заболеваниями.
Условия взятия и хранения образца: Сыворотка крови. Хранение не более 24 ч при 4–8 °С. Допускается однократное замораживание образца.
Метод исследования: ИФА, иммунотурбидиметрия, иммунонефелометрия.
Повышение концентрации С3 наблюдается при некоторых острых бактериальных, паразитарных и вирусных инфекциях, аутоиммунных и воспалительных заболеваниях.
Снижение концентрации С3 -наблюдается при врожденных дефектах комплемента, различных воспалительных и инфекционных, аутоиммунных заболеваниях, длительном голодании, при лечении цитостатиками, ионизирующем излучении.
Повышение концентрации С4 характерно для реакции острой фазы, отмечается при аутоиммунных заболеваниях, назначении некоторых лекарственных препаратов.
Снижение концентрации С4 – отмечается при врожденных дефектах системы комплемента (С4 дефицит новорожденных), некоторых аутоиммунных заболеваниях, системных васкулитах, синдроме Шегрена, трансплантации почек.
Разница между гуморальным и клеточным иммунитетом
Определение
Гуморальный иммунитет: Гуморальный иммунитет относится к компоненту адаптивного иммунитета, где В-клетки выделяют антитела, которые циркулируют в крови как растворимый белок.
Клеточный Иммунитет: Клеточно-опосредованный иммунитет относится к другому компоненту адаптивного иммунитета, который опосредован активированными антиген-специфическими Т-клетками.
Главные ячейки
Гуморальный иммунитет: Гуморальный иммунитет опосредуется В-клетками.
Клеточный Иммунитет: Клеточно-опосредованный иммунитет опосредуется Т-клетками.
Типы клеток
Гуморальный иммунитет: Гуморальный иммунитет опосредуется Т-клетками, В-клетками и макрофагами.
Клеточно-опосредованный иммунитет: Клеточно-опосредованный иммунитет опосредуется вспомогательными Т-клетками, цитотоксическими Т-клетками, природными клетками-киллерами и макрофагами.
действие
Гуморальный иммунитет: Гуморальный иммунитет действует на внеклеточные микробы и их токсины.
Клеточный Иммунитет: Клеточно-опосредованный иммунитет действует на внутриклеточные микробы, такие как вирусы, бактерии, паразиты и опухолевые клетки.
Рецепторы
Гуморальный иммунитет: Рецепторы BCR участвуют в гуморальном иммунитете.
Клеточный Иммунитет: Рецепторы TCR вовлечены в клеточный иммунитет.
Вспомогательные поверхностные молекулы
Гуморальный иммунитет: Рецепторы Igα, Igβ, CD40, CD21 и Fc являются дополнительными рецепторами гуморального иммунитета.
Клеточный Иммунитет: CD2, CD3, CD4, CD8, CD28 и интегрины являются дополнительными рецепторами клеточного иммунитета.
Роль молекул MHC
Гуморальный иммунитет: Необработанные антигены распознаются гуморальным иммунитетом.
Клеточный Иммунитет: Антигены обрабатываются и представлены комплексами MHC в клеточном иммунитете.
Секреция
Гуморальный иммунитет: В-клетки плазмы секретируют антитела в гуморальный иммунитет.
Клеточный Иммунитет: Т-клетки секретируют цитокины.
начало
Гуморальный иммунитет: Гуморальный иммунный ответ быстрый.
Клеточный Иммунитет: Клеточно-опосредованный иммунный ответ представляет собой гиперчувствительность замедленного типа.
Опухолевые клетки и трансплантаты
Гуморальный иммунитет: Гуморальный иммунитет не действует на опухолевые клетки и трансплантаты.
Клеточный Иммунитет: Клеточный иммунитет действует на опухолевые клетки и трансплантаты.
Заключение
Гуморальный иммунитет и клеточный иммунитет представляют собой два типа адаптивного иммунитета, при которых специфический иммунный ответ вырабатывается для конкретного патогена. Антитела продуцируются плазматическими Т-клетками при гуморальном иммунитете. В клеточном иммунитете Т-клетки вызывают апоптоз инфицированных клеток. Гуморальный иммунитет разрушает внеклеточные патогены, тогда как клеточный иммунитет разрушает внутриклеточные патогены. В этом разница между гуморальным и клеточным иммунитетом.
Ссылка:
1. Дженуэй, Чарльз А. и младший. «Гуморальный иммунный ответ». Иммунобиология: иммунная система в здоровье и болезни. 5-е издание, Национальная медицинская библиотека США, 1 января 1970 г.
Неспецифический иммунитет
На первой стадии после рождения человека происходит формирование неспецифического иммунитета. В этом случае защита начинает работать в ответ на проникновение инородных веществ.
Гуморальный иммунитет и борьба на клеточном уровне при неспецифической защите формируются под воздействием различных факторов в зависимости от способа возникновения иммунной реакции организма.
Естественные защитные способности организма обуславливаются механическими барьерами, которые создаются при проникновении бактерий и инфекций в различные системы. Неспецифические факторы иммунитета проявляются в виде:
- целостности кожных покровов;
- выделений, вырабатываемых различными органами (слезы, моча, слюна, мокрота);
- эпителия, ворсинок, образующих слизистую оболочку органов дыхания.
Все они предотвращают воздействие внедренных веществ на организм. Избавление от негативного влияния происходит в процессе чихания, диареи, рвоты. При правильном иммунном ответе может наблюдать повышение температуры тела, нарушение гормонального фона организма.
Биохимическая неспецифическая защита производится благодаря наличию различных факторов, к которым относятся:
- кислоты, вырабатываемые сальными железами;
- лизоцим слюны, устраняющий влияние грамположительных бактерий;
- пониженная кислотность мочи, секрета из влагалища, желудочного сока, защищающие органы от бактериального воздействия.
При неспецифической защите огромную роль играет клеточная составляющая. Работа в этом направлении в организме осуществляется:
- мононуклеарными фагоцитами (моноцитами, макрофагами тканей);
- гранулоцитами (нейтрофилами, эозинофилами, базофилами);
- клетками-киллерами.
Кроме этого среди неспецифических компонентов защитной функции выделяют:
- систему комплемента (белки сыворотки крови);
- составляющие гуморального иммунитета, к которым относят врожденные антитела сыворотки крови (разрушают грамотрицательные бактерии, белок пропердин);
- белок бета-лизин в тромбоцитах (разрушает грамположительные бактерии);
- интерфероны, способствующие защите клеток от вирусного поражения.
Иммунитет неспецифической формы имеет некоторые особенности, которые отличают его от приобретенной защиты.
- При проникновении чужеродных тел происходит активизация всех факторов естественной защиты, что приводит к возникновению побочных эффектов.
- Неспецифическая защита не обладает запоминанием возбудителя заболевания, что приводит к возможности дальнейшего его воздействия на организм.
Сила иммунного ответа
Сила иммунного ответа зависит от способности организма реагировать на попадание инфекции, токсинов или ядов. Поэтому, в зависимости от силы, различают несколько видов иммунного ответа: нормоэргический, гипоэргический и гиперэргический.
Нормоэргический ответ – это соответствие силы иммунитета силе агрессии вредных микроорганизмов с последующим устранением последних. При данном типе иммунного ответа нарушение целостности тканей в процессе воспаления умеренное и не приводит к серьезным последствиям для организма. Нормоэргический иммунный ответ присущ людям с нормальной функцией иммунной системы.
Гипоэргический ответ – когда агрессия со стороны микроорганизмов сильнее иммунитета больного. В итоге организм не в состоянии полностью ограничить размножение инфекции, что переводит заболевание в хроническое состояние. Такая форма иммунного ответа характерна для людей детского и пожилого возраста, а также для лиц с первичным и вторичным иммунодефицитами.
Гиперэргический ответ формируется на фоне сенсибилизации организма по отношению к поступившему антигену, в несколько раз превышая силу агрессии микроорганизмов. В процессе гиперэргического иммунного ответа воспалительная реакция увеличивается до такого состояния, которое может повредить здоровые тканей организма. Возникновение данного типа иммунной реакции определяется особенностями микроорганизмов, а также индивидуальными показателями самой иммунной системы организма.
Гиперэргический иммунный ответ является основой формирования аллергической реакции.
Взаимосвязь клеточной и гуморальной защиты
При клеточном иммунитете оборона опосредована клетками. Понятие о клеточном оборонном механизме было введено и развито выдающимся российским биологом И.И. Мечниковым. Благодаря ему и Паулю Эрлиху, объявившему миру о гуморальном иммунитете, сосредоточенному в плазме крове, иммунология совершила квантовый прыжок в своем развитии. Выдающиеся ученые-биологи являются обладателями Нобелевской премии.
Каждая первоначально продуцированная В-клетка имеет только один вид антитела, что делает каждую В-клетку уникальной. Это огромное количество В-клеток в организме, каждый из которых производит уникальное антитело, которое позволяет иммунной системе обнаруживать такое широкое разнообразие патогенных антигенов. В-клетки, содержащие антитела, которые распознают «собственные» антигены, разрушаются до того, как они могут созревать, не позволяя иммунной системе атаковать хозяина. Как только В-клетки созревают в костном мозге, они мигрируют в лимфатические узлы или другие лимфатические органы, где они могут начать сталкиваться с патогенами.
Клеточные и гуморальные оборонные механизмы тесно взаимосвязаны. Они не могут существовать автономно друг от друга, отличаются функциональностью. Если гуморальная защита призвана вступать в сражение с бактериями, то клеточная – с грибком, вирусом, раковыми клетками.
Клетки функциональной системы иммунного гомеостаза.
Иммунокомпетентные клетки:
a)Т-лимфоциты; b)В-лимфоциты; c)ЕК.Антигенпрезентирующие клетки:
a)макрофаги крови (моноциты) – презентируют АГ, участвуя в развитии гуморального иммунного ответа через Th2; b)нефагоцитирующие А-клетки (клетки Лангерганса, вуалевидные клетки, отростчатые клетки, дендритные клетки, тканевые макрофаги) – играют антигенпрезентирующую роль для развития клеточного иммунного ответа через Тh1, Tctl, EK. Вспомагательные клетки (тучные клетки, базофилы, эозинофилы, тромбоциты) – участвуют в развитии воспалительной реакции. По функциональной активности иммунокомпетентные клетки (ИКК) подразделяют на: Регуляторные ИККЭффекторные клетки являются непосредственными исполнителями иммунного реагирования. Они действуют на объект либо непосредственно, либо путем биосинтеза биологически активных веществ со спецефическим эффектом (иммуноглобулины).Cluster of differentiation (CD) – это показатель дифференцировки, маркер, определяющий особенности клеток иммунной системы и обладающий антигенными свойствами.В 1969 году И. Ройт ввел в иммунологию понятие Т- и и В-лимфоцитов: Т-лимфоцитыВ-лимфоцитыЦентральной клеткой иммунной системы является лимфоцит (1-4×109/л)Т-лимфоциты – клетки, отвечающие за клеточный иммунитет. Поверхностные рецепторы Т-лимфоцитов:CD2 (рецептор к эритроцитам барана). CD3 (рецепторы к антигенам). К Fc-фрагменту иммуноглобулинов.К белкам системы комлемента (но не имеют рецепторов к C3b). К интерлейкинам.Субпопуляции Т-лимфоцитов:нулевые Т-лимфоциты; Т-хелперы;эффекторы ГЗТ (ТГЗТ); цитотоксические Т-лимфоциты (Т-киллеры); Т-супрессоры; Т-клетки памяти. Т-хелперы первого типа (Th1), выделяющие ИЛ-2, ИЛ-12, ИФН-γ, ФНО-α – обеспечивают реакции Т-клеточного иммунитета. Т-хелперы второго типа (Th2), секретирующие ИЛ-4, ИЛ-5, ИЛ-10, ИЛ-13 – стимулируют синтез антител, т.е. гуморальное звено иммунной системы.ТГЗТ – эффекторыНулевые Т-лимфоцитыТ-хелперы (CD4) распознают антиген в комплексе с локализованными на мембране клеток-мишеней антигенами МНС II класса.Т-хелперыСреди них различают:Цитотоксические Т-лимфоциты (Т-киллеры)Несут на своей поверхности антиген CD8, который служит рецептором для антигенов к молекулам главного комплекса гистосовместимости (МНС) I класса. После активации антигеном Т-киллеры связываются с антигенами на поверхности клеток и, выделяя цитотоксин (белок перфорин), разрушают их. Т-киллерыуничтожают различные опухолевые клетки, клетки чужеродных трансплантантов, патологически мутированные клетки, клетки, инфицированные вирусами. Т-супрессорыиммунного ответа, подавляя активность CD4-лимфоцитов. Т-супрессоры:предотвращают развитие аутоиммунных реакций; защищают организм от нежелательных последствий иммунных реакций; обеспечивают толерантность матери к чужеродным антигенам, представленных на клетках вынашиваемого плода. Т-клетки иммунологической памяти (CD45RO)
Подробнее о Т-лимфоцитах
Это клетки, представляющие собой особый вид лимфоцитов, вырабатывающихся в тимусе. У людей так называется вилочковая железа, располагающаяся в грудной клетке чуть ниже щитовидки
В названии лимфоцитов использована первая буква этого важного органа. В костном мозге продуцируются предшественники Т-лимфоцитов
В тимусе происходит их окончательная дифференциация (формирование), в результате которой они приобретают клеточные рецепторы и маркеры.
Т-лимфоциты бывают нескольких типов:
- Т-хелперы. Название образовано от английского слова help, что означает «помощь». «Хелпер» на английском – это помощник. Такие клетки сами чужеродных агентов не уничтожают, но активируют выработку клеток-киллеров, моноцитов, цитокинов.
- Т-киллеры. Это «прирожденные» убийцы, цель которых – уничтожить клетки собственного организма, в которых поселился чужеродный агент. Этих «киллеров» существует множество вариаций. Каждая такая клетка «видит» только на какой-либо один вид патогенна. То есть Т-киллеры, реагирующие, например, на стрептококк, оставят без внимания сальмонеллу. Также они «не заметят» чужеродного «вредителя», проникшего в тело человека, но пока свободно циркулирующего в его жидких средах. Особенности действия Т-киллеров дают понять, чем клеточный иммунитет отличается от гуморального, работающего по другой схеме.
- γδ Т-лимфоциты. Их образуется очень мало, по сравнению с другими Т-клетками. Настроены они на распознавание липидных агентов.
- Т-супрессоры. Их роль – обеспечить иммунный ответ такой продолжительности и такой силы, которые требуются в каждом конкретном случае.
Фазы нормального иммунного ответа во времени
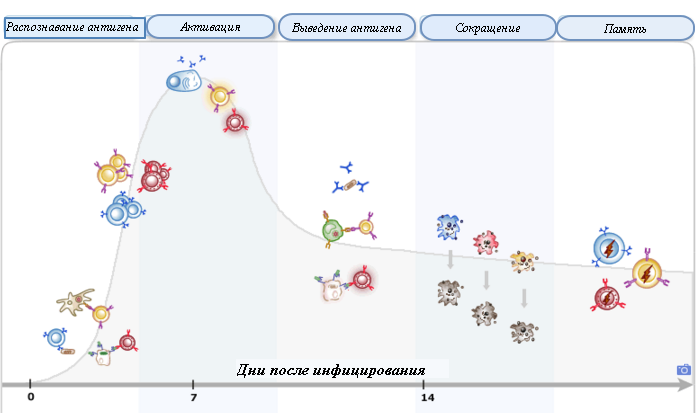
В предыдущих статьях были отражены механизмы, с помощью которых B и T лимфоциты распознают антигены, дифференцируются и в конечном итоге устраняют распознанные антигены. Эта статья имеет целью объединения всех предыдущих концепций в единую временную шкалу: адаптивные иммунные ответы соответствуют примерно той же шкале времени. Во-первых, несколько наивных лимфоцитов сталкиваются с антигеном и активируются. После активации они делятся, и популяция активированных лимфоцитов увеличивается, не отставая от растущей популяции микробов. Помните, что на начальном этапе существует только несколько наивных лимфоцитов, специфичных для любого одного антигена в организме, поэтому лимфоцитам необходимо делиться, чтобы иметь достаточное количество клеток для сильного ответ и идти в ногу с интенсивностью деления микробов. После того, как лимфоциты поделятся и дифференцируются на эффекторные типы, антиген удаляется, большинство лимфоцитов подвергается апоптозу, возвращая тело к гомеостазу. Осталось только несколько клеток памяти, готовых ответить на повторную инфекцию (рис.).
|
Фазы адаптивного иммунного ответа |
Что происходит |
|
Фаза распознавания |
Во время фазы распознавания наивные В и Т-клетки встречаются с новым микробом. Встреча инициирует процесс клональной экспансии, при которой происходит деление стимулированного лимфоцита. На рис. В-клетка узнала свободно плавающий микроб; АПК — дендритная клетка — представляет Т-клетке пептидный антиген из фагоцитированного микроба. |
| Активации | Активированные В и Т-клетки быстро делятся, образуя эффекторные клетки. В лимфоциты созревают в плазматические клетки и начинают секретировать антитела против специфического антигена. Хелперные Т- клетки деляться и их цитокины активируют макрофаги, чтобы убить антиген. Цитотоксические Т-клетки готовы к прямому уничтожению инфицированных клеток. |
| Выведение антигена |
Вовремя эффекторной фазы антитела и дифференцированные эффекторные Т- клетки устраняют антиген. |
| Память |
В финальной фазе , фазе «памяти» антиген-специфические клетки остаются в организме. При повторном экспонировании клетки памяти быстро размножаются, создавая иммунный ответ, который намного быстрее и надежнее, чем исходный ответ |
В соответствии с рисунком, при нормальном иммунном ответе пик активации адаптивного иммунного ответа достигается к 6-10 дню. Затем по мере выведения антигена количество эффекторных клеток снижается. К 14 -15 дню восстанавливается гомеостаз. Следует отметить, что это среднестатистическая шкала фаз. В норме продолжительность каждой фазы может варьироваться в зависимости от ответов на различные антигены.