Хиломикроны и лпонп переносят триацилглицеролы
Содержание:
- Признаки изменения в липидном обмене
- БИОХИМИЯ – Основные питательные вещества человека – 2016 год
- Причины нарушения липидного обмена
- Эйкозаноиды
- Что такое липиды, и на какие группы они делятся?
- Причины нарушений переваривания липидов
- Регуляция липидного обмена
- Окисление жирных кислот
- Типы нарушений
- Патологии липидного обмена
- Обмен холестерола
- Метаболизм липидов в норме и при патологии. Дисфункция жировой ткани. Ожирение
- Обмен фосфолипидов
Признаки изменения в липидном обмене
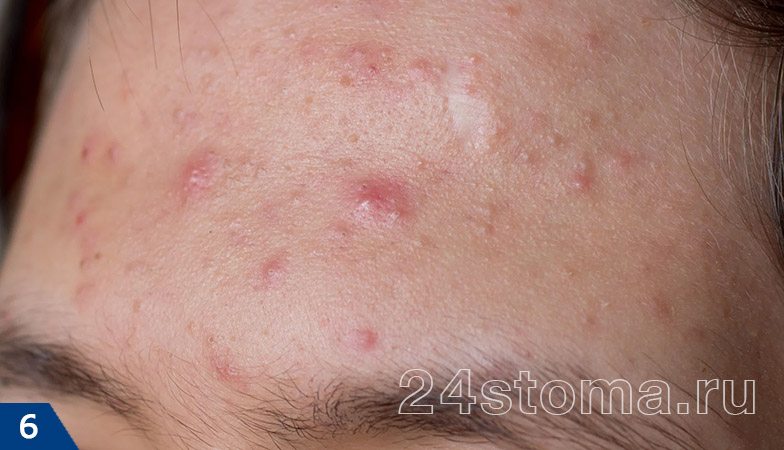
Симптомы развития гиперхолестеринемии первичной этиологии (генетической) и вторичной этиологии (приобретённой), вызывают большое количество изменений в организме пациента.
Многие симптомы можно выявить только посредством диагностического исследования инструментальными и лабораторными методиками, но существуют и такие симптомы проявления, которые можно обнаружить визуально и при применении метода пальпации:
- Формируются ксантомы на теле пациента;
- Формирование ксантелазм на глазных веках и на кожных покровах;
- Ксантомы на сухожилиях и суставах;
- Появление холестериновых отложений в уголках глазных разрезов;
- Повышается масса тела;
- Происходит увеличение селезёнки, а также печёночного органа;
- Проявляется симптоматика атеросклероза;
- Диагностируются явные признаки развития нефроза;
- Формируются обобщённые симптомы патологии эндокринной системы.
Данная симптоматика указывает на нарушение липидного обмена и увеличения индекса холестерина в составе крови.
При изменении в липидном обмене в сторону снижения липидов в плазме крови, выраженная такая симптоматика:
- Снижается масса и объём тела, что может привести к полному истощению организма — анорексии;
- Выпадение волос с головы;
- Расслоение и ломкость ногтей;
- Экземы и язвочки на кожных покровах;
- Воспалительные процессы на коже;
- Сухость кожи и отшелушивание эпидермиса;
- Патология нефроз;
- Нарушение у женщин цикла менструации;
- Женское бесплодие.
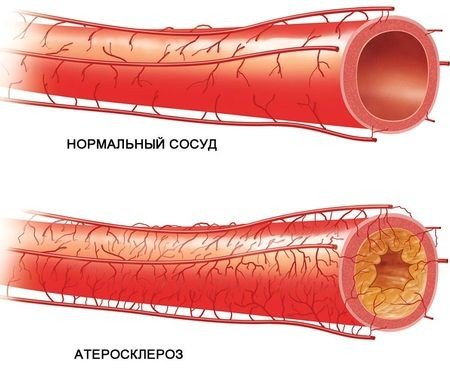
Проявляется симптоматика атеросклероза
Симптомы изменения в липидном обмене одинаковы в детском организме и в организме взрослого.
У детей чаще проявляются наружные признаки повышения индекса холестерина в крови, или же снижение концентрации липидов, а во взрослом организме внешние признаки проявляются тогда, когда патология прогрессирует.
БИОХИМИЯ – Основные питательные вещества человека – 2016 год
2.4.2. Катаболизм жиров
Использование организмом жира в качестве источника энергии начинается с его выхода из жировых депо в кровяное русло. Этот процесс называется мобилизацией жира. Мобилизация жира ускоряется под влиянием симпатической нервной системы и гормона адреналин.
Основные превращения жира происходят в печени, где имеются активные ферменты жирового обмена.
В печени жир прежде всего подвергается гидролизу и превращается, так же, как и в кишечнике, в глицерин и жирные кислоты.
Образовавшийся глицерин легко переходит в фосфоглпцерпновый альдегид, который является также промежуточным продуктом распада углеводов и поэтому вовлекается в углеводный обмен.
Жирные кислоты вначале активируются с использованием энергии АТФ и связываются со своим переносчиком – коферментом А (комплекс «жирная кислота – кофермент А» называется ацилкоферментом А):
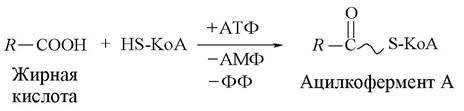
Затем ацилкофермент А с помощью еще одного переносчика – карнитина поступает в митохондрии, где происходит окисление жирной кислоты.
Окисление жирных кислот протекает в два этапа.
На первом этапе, называемом β – окислением (это название обусловлено тем, что окислению подвергается атом С жирной кислоты, находящийся в р!!!-положении углеродной цепи), от жирной кислоты, связанной с коферментом А, дважды отщепляются по два атома водорода, которые затем по дыхательной цепи передаются на молекулярный кислород. В итоге образуется вода, и за счет выделяющейся при этом энергии осуществляется синтез пяти молекул АТФ. Завершается р-окисление отщеплением от жирной кислоты двухуглеродного фрагмента в виде ацетилкофермента А (ацетил – КоА):
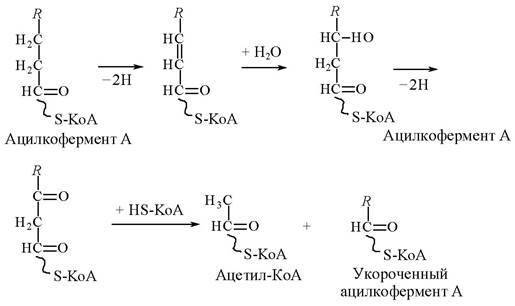
β – Окисление многократно повторяется до тех пор, пока жирная кислота полностью не превратится в ацетилкофермент А, количество молекул которого равно половине числа атомов углерода в исходной жирной кислоте. Как уже отмечалось, каждое отщепление одной молекулы ацетил – КоА сопровождается синтезом пяти молекул АТФ в ходе тканевого дыхания.
Вторым этапом окисления жирных кислот является цикл трикарбоновых кислот (ЦТК), или цикл Кребса, в котором происходит дальнейшее окисление остатка уксусной кислоты из аце- тилкофермента А до углекислого газа и воды. При окислении одной молекулы ацетил – КоА в цикле Кребса выделяется 12 молекул АТФ.
В целом окисление жирных кислот до СО2 и Н2O дает большое количество энергии. Например, в случае окисления пальмитиновой кислоты (С15Н31СООН) цикл β -окисления протекает семь раз, в результате чего образуются 35 молекул АТФ и 8 молекул ацетилкофермента А. При дальнейшем окислении 8 молекул ацетил – КоА в цикле Кребса синтезируется еще 96 молекул АТФ. Вычтя из полученной суммы молекул АТФ одну молекулу, энергия которой была затрачена на активацию жирной кислоты, получаем окончательный результат: при окислении молекулы пальмитиновой кислоты образуется 130 молекул АТФ.
Окисление жира протекает в митохондриях при обязательном использовании молекулярного кислорода, что существенно ограничивает скорость этого процесса. Поэтому за счет окисления жиров можно обеспечить энергией только работу средней мощности, но зато очень продолжительную, так как запасы жира в организме весьма значительны.
При избыточном образовании ацетилкофермента А в печени вместо цикла Кребса происходит реакция конденсации двух молекул ацетил – КоА. В результате конденсации остатки уксусной кислоты, соединяясь попарно, превращаются в кетоновые тела, а кофермент А выделяется в свободном виде:
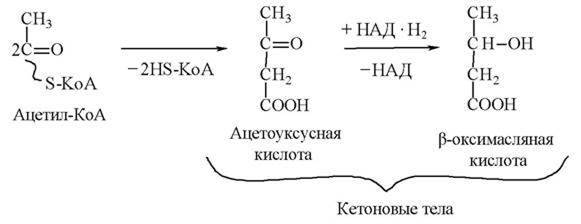
С током крови кетоновые тела поступают во все ткани.
Однако большая часть кетоновых тел извлекается из крови органами, имеющими высокие энергозатраты: миокардом, скелетными мышцами, почками.
В этих органах с участием их собственного кофермента А кетоновые тела вновь переходят в ацетилкофермент А:
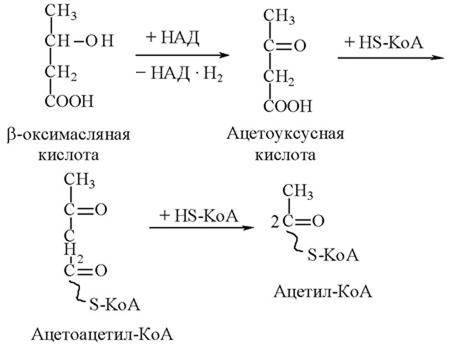
Далее ацетилкофермент А окисляется в цикле Кребса и обеспечивает эти органы энергией, необходимой для их функционирования. Особенно велика роль кетоновых тел в обеспечении организма энергией при продолжительных физических нагрузках.
При накоплении кетоновых тел в крови возможно образование ацетона:
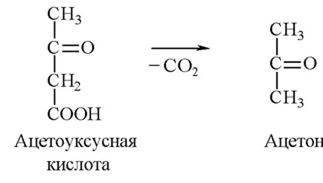
Это вещество в качестве источника энергии в организме не используется и выделяется легкими и почками.
Предыдущая
Следующая
Причины нарушения липидного обмена
В современной медицине, неправильный механизм липидного обмена носит определение дислипидемия, и возникает он, как правило, при первичном или вторичном происхождении нарушений. В первом случае (первичные нарушения), будет иметься в виду наследственный фактор, который передается от одного человека к другому, на генном уровне. Что же касается второго случая (вторичные нарушения), то к нему можно отнести любой патологический процесс, протекающий в организме пациента (даже если причина возникновения данного процесса, кроется в неправильном образе жизни больного).
Если же рассматривать первичные и вторичные нарушения метаболического процесса, как одно целое, то среди причин, влияющих на данное отклонение, можно выделить:
- Мутацию определенных генов (как единичную, так и множественную). При таком отклонении, как правило, выработка и всасывание липидов в организме существенно нарушаются, в результате чего, метаболизм также будет выполняться неправильно;
- Заболевание атеросклерозом (учитывается и наследственная болезнь). Атеросклероз, как и большинство сердечно-сосудистых патологий (таких как: ИБС, инфаркт, инсульт и т.д.) в первую очередь оказывает негативное воздействие на внутриклеточный состав крови человека, повышая тот, или иной его фермент. Ну а подобное отклонение, будет способствовать нарушению липидного обмена, с ярко выраженными признаками сердечных патологий (хроническая усталость, повышенная сонливость, легкое внезапное головокружение, артериальная гипертензия и т.д.);
- Неактивный образ жизни. Если человек не проявляет никакой активности, в течении длительного периода времени, то его миокард постепенно начинает зарастать жиром, в результате чего, норма кровяных клеток в его организме, также значительно нарушается. Ну а нарушенный коэффициент любых клеток, в свою очередь, негативно повлияет на процесс метаболизма;
 Неактивный образ жизни, как причина нарушения обмена липидов
Неактивный образ жизни, как причина нарушения обмена липидов
- Неправильное питание, вызывающее у пациента ожирение первой, второй или третей степени. Зачастую, увеличивать вес человека может пища, с высоким содержанием жиров, провоцирующая окисление жировых клеток в его организме, и вызывающая повышение холестерина в крови (в медицине такое состояние называется гиперхолестеринемия). Однако, следует также отметить, что на нарушение липидного обмена может повлиять и неправильная диета, повлекшая за собой серьезное понижение холестерина (данное состояние часто рассматривают как истощение организма);
- Сахарный диабет. Если у человека наблюдается подобный диагноз, то вероятность нарушенного метаболизма у него, явно будет выше, чем у остальных категорий больных. Ведь при подобной патологии, как правило, кровь перенасыщается глюкозой, в результате чего, любая другая клетка, входящая в состав крови, будет понемногу угнетаться, частично или полностью нарушая процесс метаболизма липидов;
- Вредные привычки (курение и чрезмерное потребление алкоголя). Как многим известно, никотин и алкоголь очень пагубно влияют на белковый и липидный клеточный состав (провоцируя их гидролитический распад), что отражается на изменении их природного количества в организме. Ну а при дисбалансе тех, или иных видов клеток, липидный обмен, также будет существенно нарушаться;
- Холестаз. При подобной патологии, центриоль в организме пациента перестает проявлять свою активность, в результате чего, его рибосома существенно нарушается. Если же вовремя не начать лечение холестаза, то он обязательно спровоцирует нарушение липидного обмена;
- Патологии разного типа, паразитирующие печень. Как показывает практика, заболевания, развитие которых происходит в области печени, также способны спровоцировать расстройство механизма липидного обмена. А связанно подобное явление, с повышением активности выработки одних клеток, и угнетением производства других.
 Поражения печени, влияющие на липидный метаболизм
Поражения печени, влияющие на липидный метаболизм
Важно! Если биохимический или общий лабораторный анализ покажет, что у пациента какая-либо группа клеток отклонилась от нормы, то это вполне можно расценивать как серьезный сигнал, свидетельствующий о возможном нарушении метаболизма в организме человека. Ну а в случае, если у больного подтвердятся вышеперечисленные патологии, то вероятность одновременного нарушения липидного обмена у него, будет практически стопроцентная
Эйкозаноиды
Основная статья: Эйкозаноиды
Эйкозаноиды, включающие в себя простагландины, тромбоксаны, лейкотриены и ряд других веществ, — высокоактивные регуляторы клеточных функций. Они имеют очень короткий Т1/2, поэтому оказывают эффекты как «гормоны местного действия», влияя на метаболизм продуцирующей их клетки по аутокринному механизму, и на окружающие клетки — по паракринному механизму. Эйкозаноиды участвуют во многих процессах: регулируют тонус гладкомышечных клеток и вследствие этого влияют на АД, состояние бронхов, кишечника, матки. Эйкозаноиды регулируют секрецию воды и натрия почками, влияют на образование тромбов. Разные типы эйкозаноидов участвуют в развитии воспалительного процесса, происходящего после повреждения тканей или инфекции. Такие признаки воспаления, как боль, отёк, лихорадка, в значительной мере обусловлены действием эйкозаноидов. Избыточная секреция эйкозаноидов приводит к ряду заболеваний, например, бронхиальной астме и аллергическим реакциям.
Субстраты для синтеза эйкозаноидов
Основным субстратом для синтеза эйкозаноидов является арахидоновая (ω-6-эйкозатетраеновая) кислота, содержащая 4 двойные связи при углеродных атомах (5, 8, 11, 14). Она может поступать с пищей или синтезироваться из линолевой кислоты. В небольших количествах для синтеза эйкозаноидов могут использоваться ω-6-эйкозатриеновая кислота с тремя двойными связями (5, 8, 11) и ω-3-эйкозапентаеновая кислота, в составе которой имеется 5 двойных связей в положениях 5, 8, 11, 14, 17. Обе минорные эйкозановые кислоты либо поступают с пищей, либо синтезируются из олеиновый и линоленовой кислот соответственно.
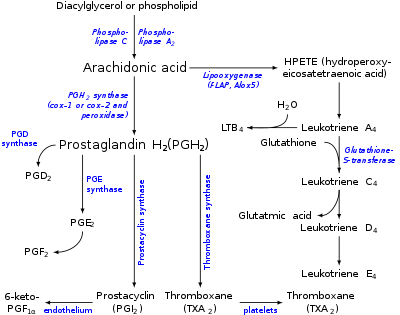
Пути биосинтеза эйкозаноидов из арахидоновой кислоты
Синтез лейкотриенов, ГЭТЕ(гидроксиэйкозатетроеноатов), липоксинов
Дополнительные сведения: Лейкотриены
Синтез лейкотриенов идёт по пути, отличному от пути синтеза простагландинов, и начинается с образования гидроксипероксидов — гидропероксидэйкозатетраеноатов (ГПЭТЕ). Эти вещества или восстанавливаются с образованием гидроксиэйкозатетроеноатов (ГЭТЕ) или превращаются в лейкотриены или липоксины. ГЭТЕ отличаются по положению гидроксильной группы у 5-го, 12-го или 15-го атома углерода, например: 5-ГЭТЕ, 12-ГЭТЕ.
Липоксины (например, основной липоксин А4) включают 4 сопряжённых двойных связи и 3 гидроксильных группы.
Синтез липоксинов начинается с действия на арахидоновую кислоту 15-липоксигеназы, затем происходит ряд реакций, приводящих к образованию липоксина А4
Клинические аспекты обмена эйкозаноидов
Медленно реагирующая субстанция при анафилаксии (МРВ-А) представляет собой смесь лейкотриенов С4, D4 и Е4. Эта смесь в 100—1000 раз более эффективна, чем гистамин или простагландины как фактор, вызывающий сокращение гладкой мускулатуры бронхов. Эти лейкотриены вместе с лейкотрином В4 повышают проницаемость кровеносных сосудов и вызывают приток и активацию лейкоцитов, а также, являются важными регуляторами при многих заболеваниях, в развитии которых участвуют воспалительные процессы или быстрые аллергические реакции (например, при бронхиальной астме).
Использование производных эйкозаноидов в качестве лекарственных средств
Хотя действие всех типов эйкозаноидов до конца не изучено, имеются примеры успешного использования лекарств — аналогов эйкозаноидов для лечения различных заболеваний. Например, аналоги PG Е1 и PG Е2 подавляют секрецию соляной кислоты в желудке, блокируя гистаминовые рецепторы II типа в клетках слизистой оболочки желудка. Эти лекарства, известные как Н2-блокаторы, ускоряют заживление язв желудка и двенадцатиперстной кишки. Способность PG Е2 и PG F2α стимулировать сокращение мускулатуры матки используют для стимуляции родовой деятельности.
Что такое липиды, и на какие группы они делятся?
Липиды – это жировые клетки, которые образуются в организме человека, а также попадают в его кровеносную систему, вместе с другими полезными веществами, во время приема пищи. В зависимости от выполняемых функций и строения, можно выделить несколько основных видов липидов:
- Фосфолипиды;
- Холестерин;
- Гликолипид;
- Триглицерид;
- Жировые кислоты.
 Холестерин, как один из видов липидов
Холестерин, как один из видов липидов
Все вышеперечисленные категории жировых клеток, также можно поделить на две основные подгруппы: хорошие и плохие липиды, разница между которыми, в первую очередь, будет наблюдаться в уровне их плотности (чем выше данный уровень у липида, тем лучше его характеристика). Однако, не зависимо от своей подгруппы, все жировые клетки, без исключения, могут принимать участие в липидном обмене, а значит, при нарушении их нормы в крови пациента, процесс метаболизма может существенно нарушаться.
Причины нарушений переваривания липидов
1. Снижение желчеобразования в результате недостаточного синтеза желчных кислот и фосфолипидов при болезнях печени, гиповитаминозах.
2. Снижение желчевыделения (обтурационная желтуха, билиарный цирроз, желчнокаменная болезнь). У детей часто причиной может быть перегиб желчного пузыря, который сохраняется и во взрослом состоянии.
3. Снижение переваривания при недостатке панкреатической липазы, который возникает при заболеваниях поджелудочной железы (острый и хронический панкреатит, острый некроз, склероз). Может возникать относительная недостаточность фермента при сниженном выделении желчи.
4. Избыток в пище катионов кальция и магния, которые связывают жирные кислоты, переводят их в нерастворимое состояние и препятствуют их всасыванию. Эти ионы также связывают желчные кислоты, нарушая их работу.
5. Снижение всасывания при повреждении стенки кишечника токсинами, антибиотиками (неомицин, хлортетрациклин).
6. Недостаточность синтеза пищеварительных ферментов и ферментов ресинтеза липидов в энтероцитах при белковой и витаминной недостаточности.
Нарушение желчевыделения
Нарушение желчеобразования и желчевыделения чаще всего связаны с хроническим избытком ХС в организме вообще и в желчи в частности, так как желчь является единственным способом его выведения.
Избыток ХС в печени возникает при увеличении количества исходного материала для его синтеза (ацетил-SКоА) и при недостаточном синтезе желчных кислот из-за снижения активности 7α-гидроксилазы (гиповитаминозы С и РР).
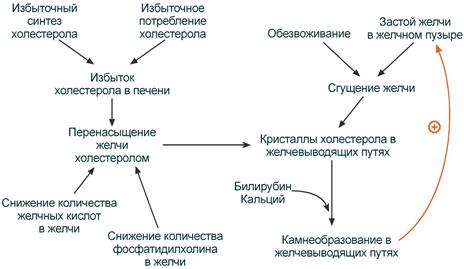
Причины нарушения формирования желчи и возникновения холелитиаза
Избыток ХС в желчи может быть абсолютным в результате избыточного синтеза и потребления или относительным. Так как соотношение желчных кислот, фосфолипидов и холестерола должно составлять 65:12:5, то относительный избыток возникает при недостаточном синтезе желчных кислот (гиповитаминозы С, В3, В5) и/или фосфатидилхолина (недостаток полиненасыщенных жирных кислот, витаминов В6, В9, В12). В результате нарушения соотношения образуется желчь, из которой холестерол, как плохо растворимое соединение, кристаллизуется. Далее к кристаллам присоединяются ионы кальция и билирубин, что сопровождается образованием желчных камней.
Застой в желчном пузыре, возникающий при неправильном питании, приводит к сгущению желчи из-за реабсорбции воды. Недостаточное потребление воды или длительный прием мочегонных средств (лекарства, кофеин-содержащие напитки, этанол) существенно усугубляет эту проблему.
Регуляция липидного обмена
Основная статья: Регуляция липидного обмена
В условиях положительного калорийного баланса значительная часть потенциальной энергии пищевых продуктов запасается в виде энергии гликогена или жира. Во многих тканях даже при нормальном питании, не говоря уже о состояниях калорийного дефицита или голодания, окисляются преимущественно жирные кислоты, а не глюкоза. Причина этого — необходимость сохранения глюкозы для тех тканей (например, для мозга или эритроцитов), которые постоянно в ней нуждаются. Следовательно, регуляторные механизмы, часто с участием гормонов, должны обеспечивать постоянное снабжение всех тканей подходящим топливом в условиях как нормального питания, так и голодания. Сбой в этих механизмах происходит при гормональном дисбалансе (например, в условиях недостатка инсулина при диабете), при нарушении метаболизма в период интенсивной лактации (например, при кетозе крупного рогатого скота) или из-за усиления обменных процессов при беременности (например, при токсикозе беременности у овец). Такие состояния представляют собой патологические отклонения при синдроме голодания; он наблюдается при многих заболеваниях, сопровождающихся снижением аппетита.
Окисление жирных кислот
Основная статья: Окисление жирных кислот
β-Окисление жирных кислот
Основная статья: β-Окисление
Процесс β-окисления высших жирных кислот (ВЖК) складывается из следующих этапов:
- активация ВЖК на наружной поверхности мембраны митохондрий при участии АТФ, кофермента А и ионов магния с образованием активной формы ВЖК (ацил — КоА).
- транспорт жирных кислот внутрь митохондрий возможен при присоединении активной формы жирной кислоты к карнитину, находящемуся на наружной поверхности внутренней мембраны митохондрий. Образуется ацил-карнитин, обладающий способностью проходить через мембрану. На внутренней поверхности комплекс распадается и карнитин возвращается на наружную поверхность мембраны.
- внутримитохондриальное окисление жирных кислот состоит из последовательных ферментативных реакций. В результате одного завершенного цикла окисления происходит отщепление от жирной кислоты одной молекулы ацетил-КоА, то есть укорочение жирнокислотной цепи на два углеродных атома. При этом в результате двух дегидрогеназных реакций восстанавливается ФАД до ФАДН2 и НАД+ до НАДН2. Таким образом завершая 1 цикл β—окисления ВЖК, в результате которого ВЖК укоротилось на 2 углеродных звена. При β-окислении выделилось 5АТФ и 12АТФ выделилось при окислении ацетил-КоА в цикле Кребса и сопряженных с ним ферментов дыхательной цепи. Окисление ВЖК будет происходить циклически одинаково, но только до последней стадии — стадии превращения масляной кислоты (бутирил-КоА), которая имеет свои особенности, которые необходимо учитывать при подсчёте суммарного энергетического эффекта окисления ВЖК, когда в результате одного цикла образуется 2 молекулы ацетил-КоА, одна из них проходила β-окисление с выделением 5АТФ, а другая нет.
ω-Окисление жирных кислот
Хотя для жирных кислот наиболее характерно β-окисление, встречаются также два других типа окисления: α-и ω-окисления. Окисление жирных кислот с длинной цепью до 2-оксикислот и затем до жирных кислот с числом атомов углерода на один меньше, чем в исходном субстрате, было показано в микросомах мозга и других тканях, а также в растениях. 2-Оксикислоты с длинной цепью являются компонентами липидов мозга.
Окисление ненасыщенных жирных кислот
Около половины жирных кислот в организме человека ненасыщенные. β-Окисление этих кислот идёт обычным путём до тех пор, пока двойная связь не окажется между третьим и четвёртым атомами углерода. Затем фермент еноил-КоА изомераза перемещает двойную связь из положения 3-4 в положение 2-3 и изменяет цис-конформацию двойной связи на транс-, которая требуется для β-окисления. В этом цикле β-окисления первая реакция дегидрирования не происходит, так как двойная связь в радикале жирной кислоты уже имеется. Далее циклы β-окисления продолжаются, не отличаясь от обычного пути.
Нарушения окисления жирных кислот
Нарушение переноса жирных кислот в митохондрии.
Скорость переноса жирных кислот внутрь митохондрий, а следовательно и скорость процесса β-окисления, зависит от доступности карнитина и скорости работы фермента карнитинацилтрансферазы I.
β-Окисление могут нарушать следующие факторы:
- длительный гемодиализ, в ходе которого организм теряет карнитин;
- длительная ацидурия, при которой карнитин выводится как основание с органическими кислотами;
- лечение больных сахарным диабетом препаратами сульфонилмочевины, ингибирующими карнитинацилтрансферазу I;
- низкая активность ферментов, синтезирующих карнитин;
- наследственные дефекты карнитинацил-трансферазы I.
Типы нарушений
В зависимости от провоцирующего фактора и патофизиологического механизма развития дислипидоза, выделяют несколько его видов:
- Первичный или врождённый основан на генетическом дефекте, который возник спонтанно ввиду мутации или наследственной передачи от одного из родителей;
- Вторичный, являющийся следствием других заболеваний;
- Алиментарный, связанный с несбалансированным питанием и употреблением большого количества жиров.
В зависимости от вида фракций, задействованных в липидном дисбалансе, нарушения могут быть:
- Чистая или изолированная гиперхолестеринемия, для которой характерно повышение уровня холестерина в кровяном русле;
- Смешанная гиперлипидемия, сочетающая увеличение числа разных видов липидов;
- Гипохолестеринемия, связанная с пониженными цифрами жиров.
По течению патологического процесса можно выделить следующие типы:
- Наследственную гиперхиломикронемию;
- Врождённую гиперхолестеринемию;
- Дис-бета-липопротеидемию;
- Комбинированную гиперлипидемию;
- Эндогенную гиперлипидемию;
- Наследственную гипертриглицеридемию.

Патологии липидного обмена
Абеталипопротеинемия
Это относительно редкое генетическое заболевание характеризуется отсутствием в плазме β-липопротеидов плотности, меньшей чем 1,063 и связано с интенсивной демиелинизацией нервных волокон. Апо-В отсутствует в плазме, так же как и в хиломикронах, ЛПОНП и ЛПНП. Уровень триацилглицеринов и холестерина плазмы очень низок. Это свидетельствует о необходимости апо-В для нормального всасывания, синтеза и транспорта триацилглицеринов и холестерина из кишечника и печени. Липиды накапливаются в клетках слизистой оболочки кишечных ворсинок, при этом наблюдается акантоцитоз — сферическая деформация эритроцитов. Более 80 % эритроцитов являются акантоцитами, или, как их иначе называют, зубчатыми эритроцитами (от греч. akantha — зубец, шип).
Кахексия
Недостаточное потребление калорий может привести и к полному исчезновению жировой ткани из подкожного и сальникового депо. Это может происходить при опухолях или хроническом инфекционном заболевании, при недостаточном питании или при метаболических нарушениях, таких, как диабет или увеличение щитовидной железы. В экспериментах было показано, что повреждение определённых областей гипоталамуса вызывает анорексию даже у предварительно голодавшего животного. Для анорексии, в происхождении которой имеет значение психогенный компонент, используют термин «anorexia nervosa» (нейрогенная анорексия).
В то время как потеря липидов тела при болезни щитовидной железы связана частично с избыточной мобилизацией резервных липидов, существенной причиной кахексии при голодании, недостаточности тиамина или диабете является сниженная способность организма синтезировать жирные кислоты из углеводных предшественников.
Атеросклероз
Основная статья: Атеросклероз
Атеросклероз (от греч. ἀθέρος — мякина, кашица + σκληρός — твёрдый, плотный) — хроническое заболевание артерий эластического и мышечно-эластического типа, возникающее вследствие нарушения липидного обмена и сопровождающееся отложением холестерина и некоторых фракций липопротеидов в интиме сосудов. Отложения формируются в виде атероматозных бляшек. Последующее разрастание в них соединительной ткани (склероз), и кальциноз стенки сосуда приводят к деформации и сужению просвета вплоть до облитерации (закупорки)
Важно различать атеросклероз от артериосклероза Менкеберга, другой формы склеротических поражений артерий, для которой характерно отложение солей кальция в средней оболочке артерий, диффузность поражения (отсутствие бляшек), развитие аневризм (а не закупорки) сосудов. Атеросклероз сосудов ведет к развитию ишемической болезни сердца.
Обмен холестерола
Холестерол — основной стероид организма животных. У взрослого человека содержание холестерола составляет 140–150 г. Около 93% стероида входит в состав мембран и 7% находится в жидкостях организма. Холестерол увеличивает микровязкость мембран и снижает их проницаемость для Н2О и водорастворимых веществ. В крови он представлен в виде свободного холестерола, входящего в оболочку липопротеинов, и его эфиров, которые вместе с ТАГ составляют внутреннее содержимое этих частиц. Содержание холестерола и его эфиров в составе хиломикронов составляет ~ 5 %, в ЛПОНП ~10%, в ЛПНП ~ 50—60% и в ЛПВП ~ 20–30 %. Концентрация холестерола в сыворотке крови взрослого человека в норме равна ~ 200 мг/дл или 5,2 ммоль/л, что соответствует холестериновому равновесию, когда количество холестерола, поступающего в организм, равно количеству холестерола выводимому из организма. Если концентрация холестерола в крови выше нормы, то это указывает на задержку его в организме и является фактором риска развития атеросклероза.
Холестерол является предшественником всех стероидов животного организма:
- жёлчных кислот, содержание которых у взрослого человека составляет около 5 г;
- стероидных гормонов: кортикостероидов, образующихся в корковом слое надпочечников, андрогенов — в семенниках и эстрогенов — в яичниках, синтез общего количества которых не превышает 40 мг/с (с — сутки);
- витамина D3, синтезирующегося в коже под действием УФ-излучению в количестве 10 мг/с.
Холестериновое равновесие поддерживается благодаря тому, что с одной стороны холестерол поступает с пищей (~ 0,3—0,5 г/с) и синтезируется в печени или других тканях (~ 0,5 г/с), а с другой — выводится с калом в виде жёлчных кислот, холестерола желчи, продуктов катаболизма стероидных гормонов, с кожным салом, в составе мембран слущенного эпителия (~ 1,0 г/с)
Метаболизм липидов в норме и при патологии. Дисфункция жировой ткани. Ожирение
В 1680 году Juan Carreno de Miranda была изображена девочка-«монстр», страдающая синдромом Prader–Willi (1954)
1. Метаболизм липидов
Термин «липиды» объединяет вещества, обладающие общим физическим свойством — гидрофобностью, то есть нерастворимостью в воде. Однако такое определение в настоящее время является не совсем корректным ввиду, того, что некоторые группы (триацилглицерины, фосфолипиды, сфинголипиды и др.) проявляют себя как амфифильные или дифильные соединения, т.е. способные растворяться как в полярных веществах (гидрофильность), так и в неполярных (гидрофобность). По структуре липиды настолько разнообразны, что у них отсутствует общий признак химического строения. Липиды разделяют на классы, в которые объединяют молекулы, имеющие сходное химическое строение и общие биологические свойства.
Основную массу липидов в организме составляют жиры — триацилглицеролы, служащие формой депонирования энергии. Жиры располагаются преимущественно в подкожной жировой ткани и выполняют также функции теплоизоляционной и механической защиты. Триацилглицеролы практически не растворимы в воде, поэтому их депонирование не сопровождается появлением осмотических проблем.
Фосфолипиды — большой класс липидов, получивший своё название из-за остатка фосфорной кислоты, придающего им свойства амфифильности. Благодаря этому свойству фосфолипиды формируют бислойную структуру мембран, в которую погружены белки. Клетки или отделы клеток, окружённые мембранами, отличаются по составу и набору молекул от окружающей среды, поэтому химические процессы в клетке разделены и ориентированы в пространстве, что необходимо для регуляции метаболизма.
Стероиды, представленные в животном мире холестеролом и его производными, выполняют разнообразные функции. Холестерол — важный компонент мембран и регулятор свойств гидрофобного слоя. Производные холестерола (жёлчные кислоты) необходимы для переваривания жиров. Стероидные гормоны, синтезируемые из холестерола, участвуют в регуляции энергетического, водно-солевого обменов, половых функций. Кроме стероидных гормонов, многие производные липидов выполняют регуляторные функции и действуют, как и гормоны, в очень низких концентрациях. Например, тромбоцитактивирующий фактор — фосфолипид особой структуры — оказывает сильное влияние на агрегацию тромбоцитов в концентрации 10-12 М; эйкозаноиды, производные полиеновых жирных кислот, вырабатываемые почти всеми типами клеток, вызывают разнообразные биологические эффекты в концентрациях не более 10-9 М. Из приведённых примеров следует, что липиды обладают широким спектром биологических функций.
В тканях человека количество разных классов липидов существенно различается. В жировой ткани жиры составляют до 75 % сухого веса. В нервной ткани липидов содержится до 50 % сухого веса, основные из них фосфолипиды и сфингомиелины (30 %), холестерол (10 %), ганглиозиды и цереброзиды (7 %). В печени общее количество липидов в норме не превышает 10-13 %.
Нарушения обмена липидов приводят к развитию многих заболеваний, но среди людей наиболее распространены два из них — ожирение и атеросклероз.
Липидный обмен включает в себя следующие процессы:
- Расщепление, переваривание и всасывание липидов в пищеварительном тракте, поступающих вместе с пищей.
- Транспорт жиров из кишечника с помощью хиломикронов.
- Обмен триацилглицеролов.
- Обмен фосфолипидов.
- Обмен холестерола.
- Взаимопревращения жирных кислот и кетоновых тел.
- Липогенез.
- Катаболизм липидов — липолиз.
- Катаболизм жирных кислот.
Печень является главным местом синтеза жирных кислот, жиров, кетоновых тел и холестерина. Жиры могут также синтезироваться в жировой ткани, однако её основной функцией остаётся депонирование липидов.
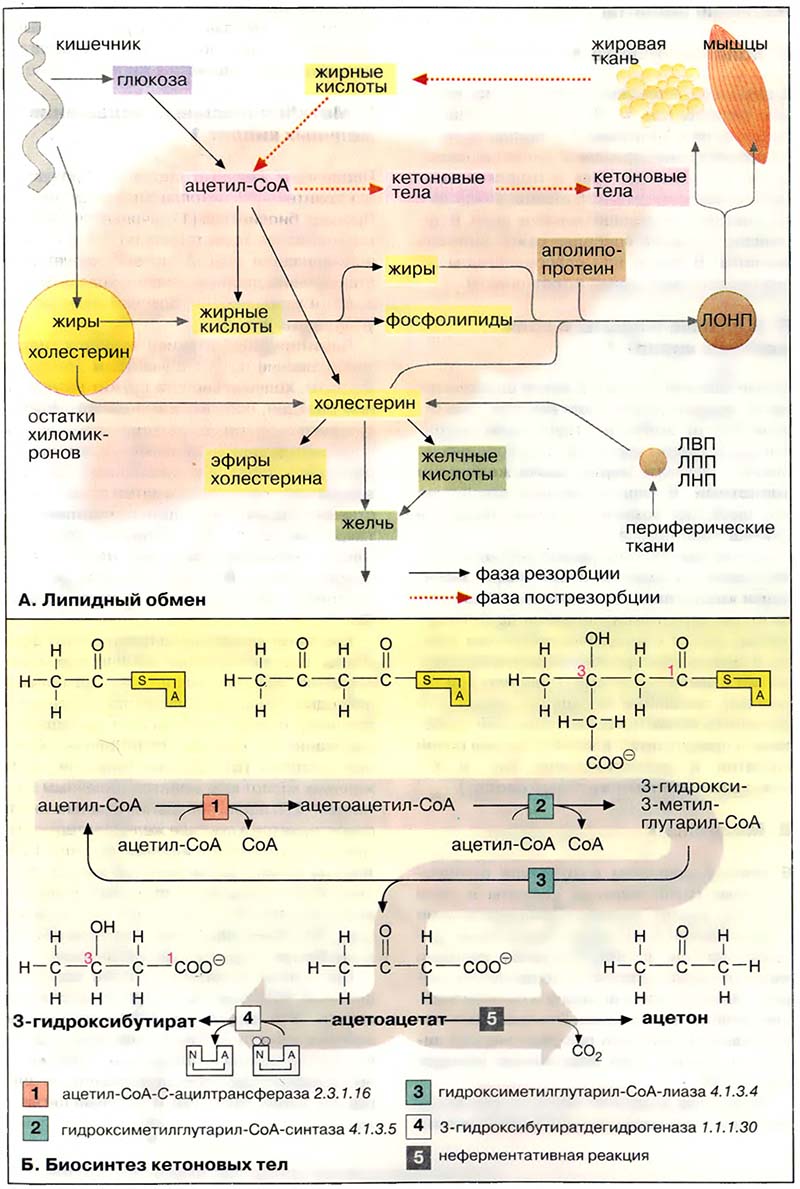
Обмен фосфолипидов
Фосфолипиды выполняют ряд важных биологических функций. Как большинство полярных липидов, они являются амфифильными соединениями, несущими гидрофобные и гидрофильные группы. Некоторые фосфолипиды, например фосфатидилхолин, представляют собой диполярные ионы, обладающие катионной и анионной группами, и являются основными компонентами клеточных мембранных систем. Например, в миелиновом волокне нерва фосфолипиды и цереброзиды составляют приблизительно 60 % сухого веса.
Распределение и обмен
Среди липидов тела фосфолипиды распределены неравномерно. Богатыми источниками фосфолипидов являются липиды тканей различных желез, в особенности печени, а также плазма крови, где они могут составлять до половины всех липидов. Фосфолипиды являются также преобладающими липидами в желтках птичьих яиц и в семенах бобовых растений. Обмен различных фосфолипидов в определённых местах животного организма изучали с использованием различных изотопов, наиболее часто 32Р. Период полупревращения этих липидов колеблется от менее одного дня для фосфатидилхолина печени до более 200 сут для фосфатидилэтаноламина мозга.